El 27 d’octubre de 2025 es va publicar un article científic molt interessant i esperançador a llarg termini. Per aquest motiu hem volgut portar-lo a aquesta sèrie d’articles divulgatius que estem desenvolupant amb la Fundació Catalana de ELA Miquel Valls. L’article és obra de Mandi Galdeman com a primer autor i de Stefan M. Pulst com a darrer autor, ambdós del Departament de Neurologia de la Universitat de Utah. El treball porta per títol «L’acció dirigida a STAU1 prevé la senyalització apoptòtica de p53 en la neurodegeneració»¹.
És important remarcar que aquest estudi s’ha realitzat en cèl·lules i models animals. Per aquest motiu, ajuda a entendre millor els mecanismes de la malaltia, però no constitueix un tractament disponible per als pacients.²
Abans d’entrar en els detalls de la recerca, convé aclarir alguns conceptes bàsics: què és l’apoptosi? I què són exactament STAU1 i p53?
L’apoptosi és el procés mitjançant el qual una cèl·lula duu a terme una mort autoprogramada. Dins la cèl·lula s’activen vies moleculars que en provoquen la destrucció controlada, generant fragments envoltats de membrana que eviten danyar les cèl·lules veïnes. Aquest mecanisme és essencial per eliminar cèl·lules danyades o que ja no funcionen correctament, també al sistema nerviós³.
Pel que fa a p53, és una molècula clau en el funcionament cel·lular. En neurones, la seva activació pot tenir efectes diversos segons el context i no sempre condueix a la mort cel·lular⁴. En general, p53 pot frenar la divisió cel·lular, activar la reparació de l’ADN o, si el dany és massa gran, desencadenar l’apoptosi mitjançant unes proteïnes anomenades caspases⁵. A més, p53 és un important supressor de tumors perquè evita que cèl·lules disfuncionals o alterades es divideixin de manera descontrolada⁵.
Quant a STAU1, és una proteïna que s’uneix al citoesquelet i als ARN missatgers (ARNm), les molècules que contenen les instruccions per fabricar proteïnes. Aquesta unió regula on es troben aquests ARNm dins la cèl·lula i possiblement quines proteïnes es produeixen⁶. En diverses malalties neurodegeneratives s’ha observat que els nivells d’STAU1 es troben anormalment elevats¹. Entre aquestes malalties hi ha l’Esclerosi Lateral Amiotròfica (ELA) i la Demència Frontotemporal (DFT) associades a l’expansió del gen C9orf72, una de les causes genètiques més freqüents de les formes familiars d’aquestes patologies, tot i que aquesta variant genètica no és present en tots els casos⁷.
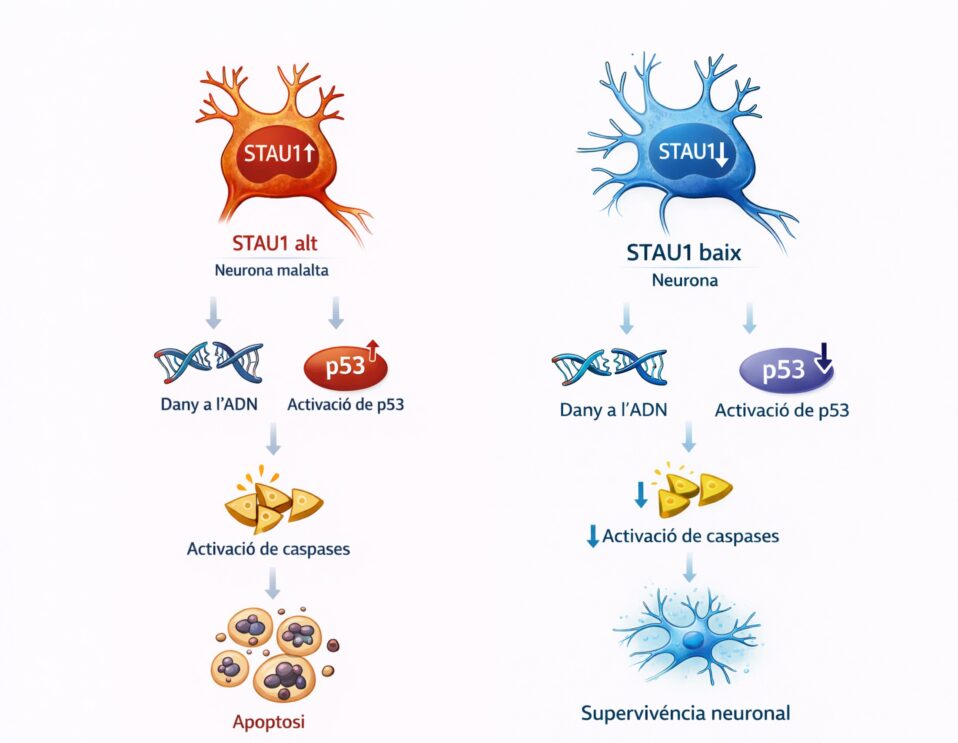
Els autors introdueixen el treball que us presentem indicant que l’apoptosi associada a p53 pot contribuir a la progressió de malalties neurodegeneratives⁸. En estudis previs, els autors havien mostrat que els nivells d’STAU1 es troben patològicament augmentats en múltiples trastorns neurològics, i que disminuir STAU1 reduïa la mort neuronal i la simptomatologia en models animals d’ELA, DFT i Atàxia Espinocerebel·losa de tipus 2¹. Tanmateix, no se’n coneixien els mecanismes moleculars.
En aquest nou estudi, els investigadors mostren que la reducció d’STAU1 pot disminuir la senyalització pro-apoptòtica associada a p53 i el dany a l’ADN en diferents models cel·lulars i animals¹. En altres paraules, nivells elevats d’STAU1 podrien contribuir al mal funcionament cel·lular, mentre que reduir-los sembla protegir les cèl·lules en determinades condicions experimentals.
Per estudiar aquest mecanisme, van analitzar quins gens estaven actius en cèl·lules amb STAU1 reduïda mitjançant una tècnica anomenada transcriptòmica⁹. En comparar els resultats amb els del control sense STAU1 reduïda, van observar que amb la reducció d’STAU1 s’activaven menys gens relacionats amb la mort cel·lular¹.
Posteriorment, en un altre experiment van exposar aquestes cèl·lules a substàncies que habitualment provoquen apoptosi. Les cèl·lules amb menys STAU1 van resultar ser més resistents a la mort cel·lular¹. També van comprovar que reduir STAU1 disminuïa el dany a l’ADN i l’activació de p53 després dels tractaments amb les substàncies. De la mateixa manera, resultats similars es van observar en fibroblasts humans (cèl·lules de la pell) procedents de pacients¹.
Per verificar si aquest efecte també es produïa en neurones, els investigadors van generar neurones al laboratori a partir de cèl·lules adultes reprogramades per tornar-les a un estat similar al de les cèl·lules mare, un model que permet estudiar neurones humanes sense necessitat d’obtenir-les directament del cervell¹⁰. En aquestes neurones, la reducció d’STAU1 també disminuïa l’apoptosi dependent de p53 i el dany a l’ADN¹. A més, es van observar uns resultats similars en estudiar neurones del còrtex cerebral de ratolins modificats genèticament per produir menys STAU1¹, és a dir, van obtenir resultats similars també en un model animal complex i viu.
Fins aquí, el missatge principal és que reduir STAU1 sembla protegir les neurones del dany i de la mort cel·lular en diversos models experimentals in vitro i in vivo.
Finalment, els investigadors van analitzar si aquest efecte també es produïa en el context de la mutació C9orf72⁷. En fibroblasts de pacients amb aquesta mutació crescuts al laboratori, reduir STAU1 va disminuir marcadors associats a l’apoptosi¹. A més, en models de ratolí amb la mutació C9orf72, la reducció d’STAU1 es va associar amb nivells més baixos de proteïnes relacionades amb la mort cel·lular, resultats en línia amb tots els mostrats prèviament¹.
Per acabar, els autors conclouen que reduir STAU1 pot protegir contra el dany a l’ADN i l’apoptosi associada a p53 en diversos models de neurodegeneració¹. També esmenten que aquest coneixement podria contribuir al desenvolupament de noves estratègies terapèutiques en el futur, tot i que cal molta més investigació abans que això es pugui traduir en tractaments aplicables a persones². També assenyalen que cal estudiar amb cautela els possibles efectes a llarg termini de reduir STAU1, ja que l’apoptosi és un procés necessari per eliminar cèl·lules danyades i p53 és essencial per prevenir el desenvolupament de tumors⁵. Per aquest motiu, probablement es continuarà investigant aquesta línia de recerca per determinar si STAU1 pot arribar a ser una diana terapèutica segura i efectiva.
Concloent, aquest estudi no descriu una un nou tractament per als pacients amb ELA/DFT, però sí que representa un avenç important en la comprensió dels mecanismes biològics de la malaltia i identifica un mecanisme que podria ajudar a desenvolupar futures teràpies.
Autors
Pol Mengod Soler1 i Dr. Pol Andrés Benito2
- Investigador Predoctoral al grup de Neurogenètica i Malalties Neurològiques del Centre d’Investigació Biomèdica de Bellvitge (IDIBELL).
- Investigador Principal al Grup d’Estudi de Cognició i Conducta de l’Institut de Recerca Biomèdica de Lleida (IRBLleida)

Referències
- Gandelman, M., Paul, S., Figueroa, K.P. et al. Targeting STAU1 prevents p53 apoptotic signalling in neurodegeneration. Cell Death Dis 16, 761 (2025). https://doi.org/10.1038/s41419-025-08067-0
- van der Worp, H.B., Howells, D.W., Sena, E.S. et al. Can animal models of disease reliably inform human studies? PLoS Med 7, e1000245 (2010). https://doi.org/10.1371/journal.pmed.1000245
- Hollville, E., Romero, S.E. & Deshmukh, M. Apoptotic cell death regulation in neurons. FEBS J 286, 3276–3298 (2019). https://doi.org/10.1111/febs.14970
- Tedeschi, A. & Di Giovanni, S. The non-apoptotic role of p53 in neuronal biology: enlightening the dark side of the moon. EMBO Rep 10, 576–583 (2009). https://doi.org/10.1038/embor.2009.89
- Hafner, A., Bulyk, M.L., Jambhekar, A. & Lahav, G. The multiple mechanisms that regulate p53 activity and cell fate. Nat Rev Mol Cell Biol 20, 199–210 (2019). https://doi.org/10.1038/s41580-019-0110-x
- Héraud-Farlow, J.E. & Kiebler, M.A. The multifunctional Staufen proteins: conserved roles from neurogenesis to synaptic plasticity. Trends Neurosci 37, 470–479 (2014). https://doi.org/10.1016/j.tins.2014.05.009
- DeJesus-Hernandez, M., Mackenzie, I.R., Boeve, B.F. et al. Expanded GGGGCC hexanucleotide repeat in noncoding region of C9ORF72 causes chromosome 9p-linked FTD and ALS. Neuron 72, 245–256 (2011). https://doi.org/10.1016/j.neuron.2011.09.011
- Lei, L., Sun, S., Zhang, S. et al. P53 protein and diseases in the central nervous system. Front Genet 13, 1051395 (2022). https://doi.org/10.3389/fgene.2022.1051395
- Wang, Z., Gerstein, M. & Snyder, M. RNA-Seq: a revolutionary tool for transcriptomics. Nat Rev Genet 10, 57–63 (2009). https://doi.org/10.1038/nrg2484
- Shi, Y., Kirwan, P., Smith, J. et al. Human cerebral cortex development from pluripotent stem cells to functional excitatory synapses. Nat Neurosci 15, 477–486 (2012). https://doi.org/10.1038/nn.3041