El 27 de octubre de 2025 se publicó un artículo científico muy interesante y esperanzador a largo plazo. Por este motivo hemos querido traerlo a esta serie de artículos divulgativos que estamos desarrollando con la Fundación Catalana de ELA Miquel Valls. El artículo es obra de Mandi Galdeman como primer autor y de Stefan M. Pulst como último autor, ambos del Departamento de Neurología de la Universidad de Utah. El trabajo lleva por título «La acción dirigida a STAU1 previene la señalización apoptótica de p53 en la neurodegeneración»¹.
Es importante remarcar que este estudio se ha realizado en células y modelos animales. Por este motivo, ayuda a comprender mejor los mecanismos de la enfermedad, pero no constituye un tratamiento disponible para los pacientes².
Antes de entrar en los detalles de la investigación, conviene aclarar algunos conceptos básicos: ¿qué es la apoptosis? ¿Y qué son exactamente STAU1 y p53?
La apoptosis es el proceso mediante el cual una célula lleva a cabo una muerte autoprogramada. Dentro de la célula se activan vías moleculares que provocan su destrucción controlada, generando fragmentos rodeados de membrana que evitan dañar a las células vecinas. Este mecanismo es esencial para eliminar células dañadas o que ya no funcionan correctamente, también en el sistema nervioso³.
En cuanto a p53, es una molécula clave en el funcionamiento celular. En neuronas, su activación puede tener efectos diversos según el contexto y no siempre conduce a la muerte celular⁴. En general, p53 puede frenar la división celular, activar la reparación del ADN o, si el daño es demasiado grande, desencadenar la apoptosis mediante unas proteínas llamadas caspasas⁵. Además, p53 es un importante supresor tumoral porque evita que células disfuncionales o alteradas se dividan de manera descontrolada⁵.
Respecto a STAU1, es una proteína que se une al citoesqueleto y a los ARN mensajeros (ARNm), las moléculas que contienen las instrucciones para fabricar proteínas. Esta unión regula dónde se localizan estos ARNm dentro de la célula y posiblemente qué proteínas se producen⁶. En diversas enfermedades neurodegenerativas se ha observado que los niveles de STAU1 se encuentran anormalmente elevados¹. Entre estas enfermedades se encuentran la Esclerosis Lateral Amiotrófica (ELA) y la Demencia Frontotemporal (DFT) asociadas a la expansión del gen C9orf72, una de las causas genéticas más frecuentes de las formas familiares de estas patologías, aunque esta variante genética no está presente en todos los casos⁷.
Los autores introducen el trabajo que presentamos indicando que la apoptosis asociada a p53 puede contribuir a la progresión de enfermedades neurodegenerativas⁸. En estudios previos, los autores habían mostrado que los niveles de STAU1 se encuentran patológicamente aumentados en múltiples trastornos neurológicos, y que disminuir STAU1 reducía la muerte neuronal y la sintomatología en modelos animales de ELA, DFT y Ataxia Espinocerebelosa tipo 2¹. Sin embargo, no se conocían los mecanismos moleculares implicados.
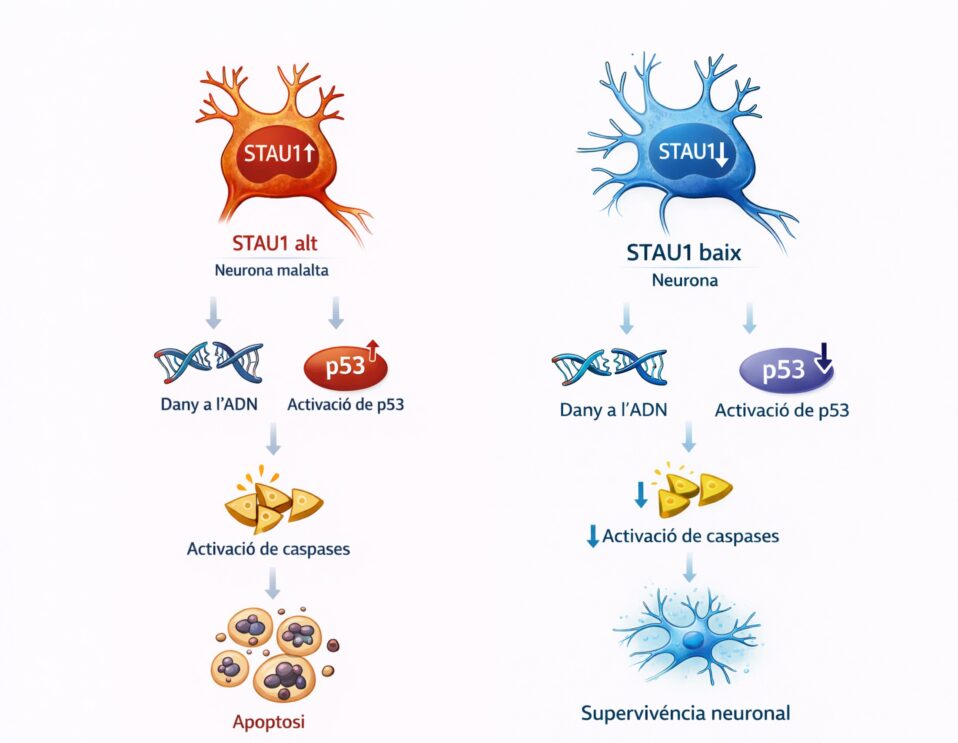
En este nuevo estudio, los investigadores muestran que la reducción de STAU1 puede disminuir la señalización proapoptótica asociada a p53 y el daño en el ADN en diferentes modelos celulares y animales¹. En otras palabras, niveles elevados de STAU1 podrían contribuir al mal funcionamiento celular, mientras que reducirlos parece proteger a las células en determinadas condiciones experimentales.
Para estudiar este mecanismo, analizaron qué genes estaban activos en células con STAU1 reducida mediante una técnica llamada transcriptómica⁹. Al comparar los resultados con los del control sin reducción de STAU1, observaron que con la reducción de STAU1 se activaban menos genes relacionados con la muerte celular¹.
Posteriormente, en otro experimento expusieron estas células a sustancias que habitualmente provocan apoptosis. Las células con menos STAU1 resultaron ser más resistentes a la muerte celular¹. También comprobaron que reducir STAU1 disminuía el daño en el ADN y la activación de p53 tras los tratamientos con dichas sustancias. Del mismo modo, se observaron resultados similares en fibroblastos humanos (células de la piel) procedentes de pacientes¹.
Para verificar si este efecto también se producía en neuronas, los investigadores generaron neuronas en el laboratorio a partir de células adultas reprogramadas para devolverlas a un estado similar al de las células madre, un modelo que permite estudiar neuronas humanas sin necesidad de obtenerlas directamente del cerebro¹⁰. En estas neuronas, la reducción de STAU1 también disminuía la apoptosis dependiente de p53 y el daño en el ADN¹. Además, se observaron resultados similares al estudiar neuronas del córtex cerebral de ratones modificados genéticamente para producir menos STAU1¹, es decir, obtuvieron resultados similares también en un modelo animal complejo y vivo.
Hasta aquí, el mensaje principal es que reducir STAU1 parece proteger a las neuronas del daño y de la muerte celular en diversos modelos experimentales in vitro e in vivo.
Finalmente, los investigadores analizaron si este efecto también se producía en el contexto de la mutación C9orf72⁷. En fibroblastos de pacientes con esta mutación cultivados en laboratorio, reducir STAU1 disminuyó marcadores asociados a la apoptosis¹. Además, en modelos de ratón con la mutación C9orf72, la reducción de STAU1 se asoció con niveles más bajos de proteínas relacionadas con la muerte celular, resultados en línea con todos los mostrados previamente¹.
Para concluir, los autores señalan que reducir STAU1 puede proteger frente al daño en el ADN y la apoptosis asociada a p53 en diversos modelos de neurodegeneración¹. También mencionan que este conocimiento podría contribuir al desarrollo de nuevas estrategias terapéuticas en el futuro, aunque se necesita mucha más investigación antes de que pueda traducirse en tratamientos aplicables a personas². Asimismo, indican que es necesario estudiar con cautela los posibles efectos a largo plazo de reducir STAU1, ya que la apoptosis es un proceso necesario para eliminar células dañadas y p53 es esencial para prevenir el desarrollo de tumores⁵. Por este motivo, probablemente se seguirá investigando esta línea para determinar si STAU1 puede llegar a ser una diana terapéutica segura y eficaz.
En conclusión, este estudio no describe un nuevo tratamiento para los pacientes con ELA/DFT, pero sí representa un avance importante en la comprensión de los mecanismos biológicos de la enfermedad e identifica un mecanismo que podría ayudar a desarrollar futuras terapias.
Autores
Pol Mengod Soler¹ y Dr. Pol Andrés Benito²
1.Investigador Predoctoral en el grupo de Neurogenética y Enfermedades Neurológicas del Centro de Investigación Biomédica de Bellvitge (IDIBELL).
2.Investigador Principal en el Grupo de Estudio de Cognición y Conducta del Instituto de Investigación Biomédica de Lleida (IRBLleida).

Referencias
- Gandelman, M., Paul, S., Figueroa, K.P. et al. Targeting STAU1 prevents p53 apoptotic signalling in neurodegeneration. Cell Death Dis 16, 761 (2025). https://doi.org/10.1038/s41419-025-08067-0
- van der Worp, H.B., Howells, D.W., Sena, E.S. et al. Can animal models of disease reliably inform human studies? PLoS Med 7, e1000245 (2010). https://doi.org/10.1371/journal.pmed.1000245
- Hollville, E., Romero, S.E. & Deshmukh, M. Apoptotic cell death regulation in neurons. FEBS J 286, 3276–3298 (2019). https://doi.org/10.1111/febs.14970
- Tedeschi, A. & Di Giovanni, S. The non-apoptotic role of p53 in neuronal biology: enlightening the dark side of the moon. EMBO Rep 10, 576–583 (2009). https://doi.org/10.1038/embor.2009.89
- Hafner, A., Bulyk, M.L., Jambhekar, A. & Lahav, G. The multiple mechanisms that regulate p53 activity and cell fate. Nat Rev Mol Cell Biol 20, 199–210 (2019). https://doi.org/10.1038/s41580-019-0110-x
- Héraud-Farlow, J.E. & Kiebler, M.A. The multifunctional Staufen proteins: conserved roles from neurogenesis to synaptic plasticity. Trends Neurosci 37, 470–479 (2014). https://doi.org/10.1016/j.tins.2014.05.009
- DeJesus-Hernandez, M., Mackenzie, I.R., Boeve, B.F. et al. Expanded GGGGCC hexanucleotide repeat in noncoding region of C9ORF72 causes chromosome 9p-linked FTD and ALS. Neuron 72, 245–256 (2011). https://doi.org/10.1016/j.neuron.2011.09.011
- Lei, L., Sun, S., Zhang, S. et al. P53 protein and diseases in the central nervous system. Front Genet 13, 1051395 (2022). https://doi.org/10.3389/fgene.2022.1051395
- Wang, Z., Gerstein, M. & Snyder, M. RNA-Seq: a revolutionary tool for transcriptomics. Nat Rev Genet 10, 57–63 (2009). https://doi.org/10.1038/nrg2484
- Shi, Y., Kirwan, P., Smith, J. et al. Human cerebral cortex development from pluripotent stem cells to functional excitatory synapses. Nat Neurosci 15, 477–486 (2012). https://doi.org/10.1038/nn.3041